Ключевое отличие: атомная масса - это просто масса определенного изотопа или объединенная масса протонов, нейтронов и электронов атома. Атомный номер - это число протонов, которое находится в ядре элемента.
Посмотрим правде в глаза, химия сбивает с толку, различное количество элементов, атомных номеров, связей, массы, веса, атомов и т. Д. Все эти слова начинают расплываться через определенное время, что человек больше не может отличить одно от другого. Атомная масса и атомный номер - это два таких слова, которые часто путают и используют взаимозаменяемо.
Атомная масса - это масса атома, когда он находится в покое. Это потому, что когда атом движется с очень высокой скоростью, он имеет тенденцию к увеличению массы. Хотя согласно определению, атомная масса - это масса всех протонов, нейтронов и электронов, электроны слишком малы, чтобы иметь какое-либо существенное различие в атомной массе. Большинство элементов периодической таблицы имеют изотопы, и из-за разницы в количестве нейтронов масса каждого изотопа также изменяется.
Атомная масса выражается в атомных единицах массы или amu. Одна атомная единица массы равна 1/12 массы углерода-12. Когда масса атома делится на 1/12 от массы углерода-12, получается относительная масса элемента. Тем не менее, относительная масса объекта фактически является атомным весом элемента, так как она рассчитывается с учетом всех изотопов. Хотя это не следует считать атомной массой элемента.

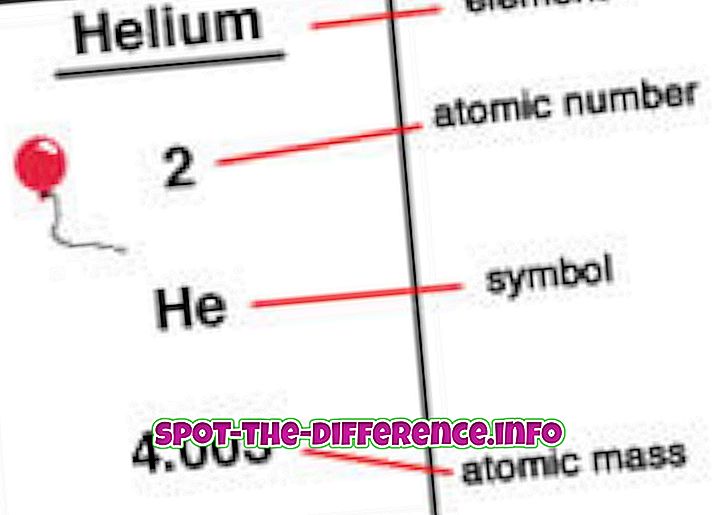
Атомный номер - это число протонов, которое находится в ядре элемента. Когда атом нейтрален, это означает, что он имеет одинаковое количество протонов и электронов. Атомный номер обозначается буквой Z. Поскольку каждый элемент имеет разное количество протонов, этот номер также используется для представления элемента. Изотопы обычно имеют один и тот же атомный номер, но классифицируются по их атомной массе, например, углерод-12, углерод-13.
Элементы располагаются в порядке атомного номера в периодической таблице. Атомный номер указан в левом верхнем углу элемента как верхний индекс. Атомные номера могут помочь разгласить информацию об элементе, и многие люди могут увидеть атомный номер и указать, что это за элемент. Он также сообщает, где в периодической таблице он может быть размещен и является ли он жидким, газообразным или твердым. Атомный номер также дает информацию о заряде ядра, степени окисления, поведении связи, заряде иона и т. Д.